【高校化学】酸化数の求め方とルールをわかりやすく徹底解説!酸化数は実はとても簡単!

共通テストによく出る、解くためには酸化数を求める必要がある問題。
酸化数をすらすらと求めることができれば解ける問題の幅が広がるので、ぜひともマスターしたいですよね。
今回はルールに基づいた酸化数の求め方について、わかりやすく徹底解説していきたいと思います。
ぜひ最後までご覧ください。
⭐︎ 酸化数とは
酸化数とは、原子のもつ本来の電子数から、電子がどれだけ増減をしたのかを表した値です。
酸化数は原理をふまえても求めることができますが、原理をふまえて求めようとすると電子式を書かなくてはいけなくなり、夜が明けるほどの時間がかかってしまいます。
なので、酸化数は論理的に考えて導くのではなく、ルールを覚えて、ルール通りに求めていく必要があります。
(原理が知りたい人はこちら→◎)
今回は酸化数のルールについて、わかりやすく解説していきたいと思います。
⭐︎ 酸化数の求めるためのルール
<酸化数を求めるための基本ルール>
単体の場合 → 酸化数は「0」である。
化合物の場合 → 各原子の酸化数を全部足したときの和は0である。
イオンの場合 → 各原子の酸化数を全部足したときの和はイオンの価数になる。
まずは、上の3つのどのパターンに当てはまるか考えます。
<酸化数を求めるための追加ルール>
・単体以外の水素の酸化数は固定で「+1」、酸素の酸化数は「ー2」。
・単体の時以外では、イオンになった時のイオンの価数が酸化数となる。
基本ルールでどのパターンか確認した後、追加ルールに基づいて酸化数を求めていきます。
⭐︎ 例題
それでは実際にルールに基づいて、下線部の原子の酸化数を求めていきましょう。
全部で4問あります。

<解説>
①の塩素は単体です。
単体の場合は酸化数はゼロなので、答えは0になります。
②の塩化水素は化合物です。
化合物の場合は、全ての酸化数を足したものがゼロになります。
水素は固定で+1なので、塩素の酸化数は−1となります。

③ はイオンです。
イオンなので、イオンの価数が酸化数の総和となります。
硫酸イオンの価数は−2なので、Sが1個とOが4個分の酸化数を足したら合計がー2になるはずです。
今回求めたいのはSなので、Sの酸化数をxとおくと、酸素は固定でー2なので以下のような方程式ができます。

よって、Sの酸化数は+6です。
酸化数を答える際はプラスの場合も符号が必要なので注意しましょう。
④は化合物です。
化合物の場合は、全ての酸化数を足したものがゼロになります。
酸素は固定でー2です。また、カリウムはイオンになるとK +なので、カリウムの酸化数は価数と同じ+1となります。
今回求めたいのはMnなので、Mnの酸化数をxとおくと以下のような方程式ができます。
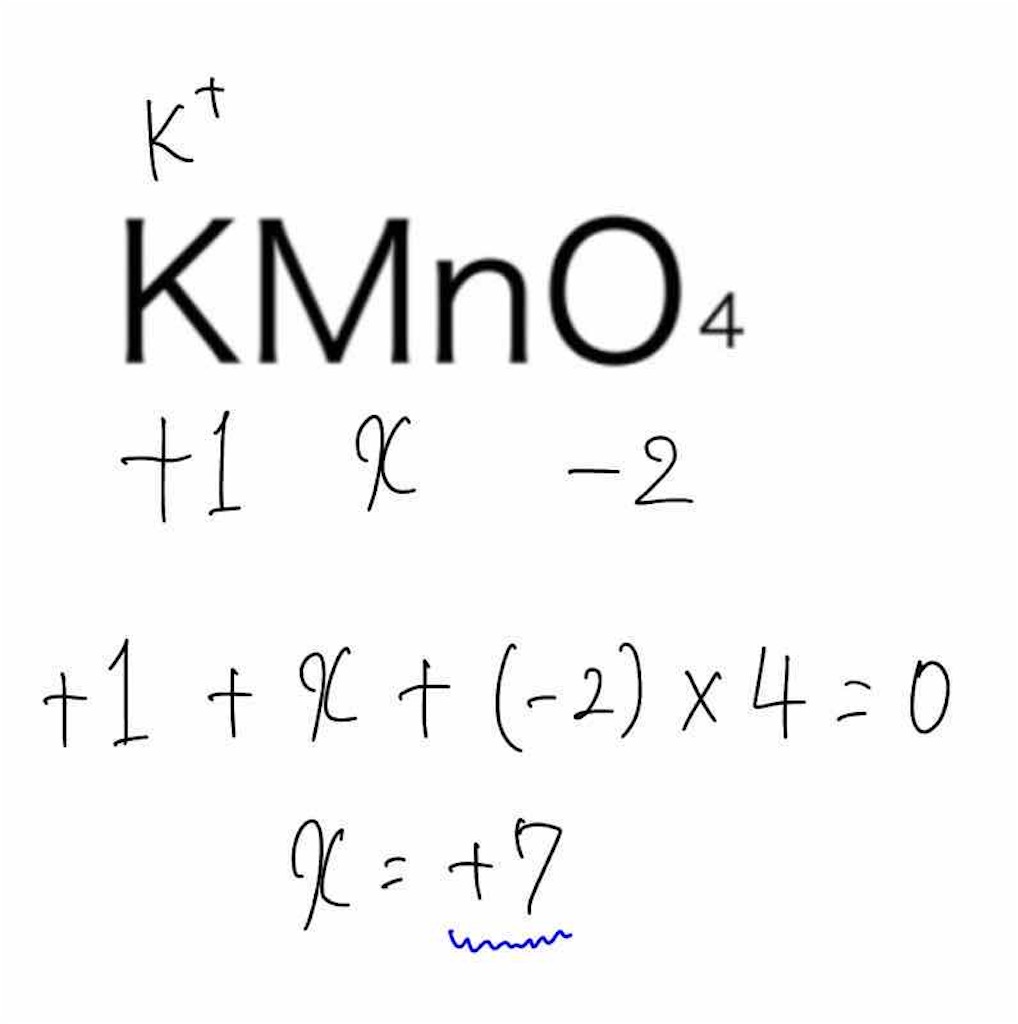
よって、Mnの酸化数は+7となります。
筆者は方程式でやりましたが、暗算でできる人は暗算でもいいと思います。
⭐︎ まとめ
酸化数とは、原子のもつ本来の電子数から、電子がどれだけ増減をしたのかを表した値のこと。
<酸化数を求めるための基本ルール>
単体の場合 → 酸化数は「0」である。
化合物の場合 → 各原子の酸化数を全部足したときの和は0である。
イオンの場合 → 各原子の酸化数を全部足したときの和はイオンの価数になる。
<酸化数を求めるための追加ルール>
・単体以外の水素の酸化数は固定で「+1」、酸素の酸化数は「ー2」。
・単体の時以外では、イオンになった時のイオンの価数が酸化数となる。
まずは基本ルールでどのタイプに当てはまるかを考え、その後、追加ルールに則って酸化数を求める。
化学の偏差値10アップを目指して、頑張りましょう。
またぜひ、当ブログにお越しください。