【高校化学】化学結合の見分け方を徹底解説!分子結晶と共有結合性の結晶の違いは?

一体何が違うのか、どうやって見分けるのかわからなくなってしまいますよね。
今回は、化学結合の見分け方を原理を含めて徹底解説していきたいと思います。
違いが分かりづらい分子結晶と共有結合性の結晶についても解説していますので、ぜひ最後までご覧ください。
⭐︎ 結合の種類
結合の種類は、全部で3種類です。
みなさん、周期表を思い出してください。
元素は金属元素(だいたい周期表の左側)と非金属元素(だいたい周期表の右側)に分けることができました。
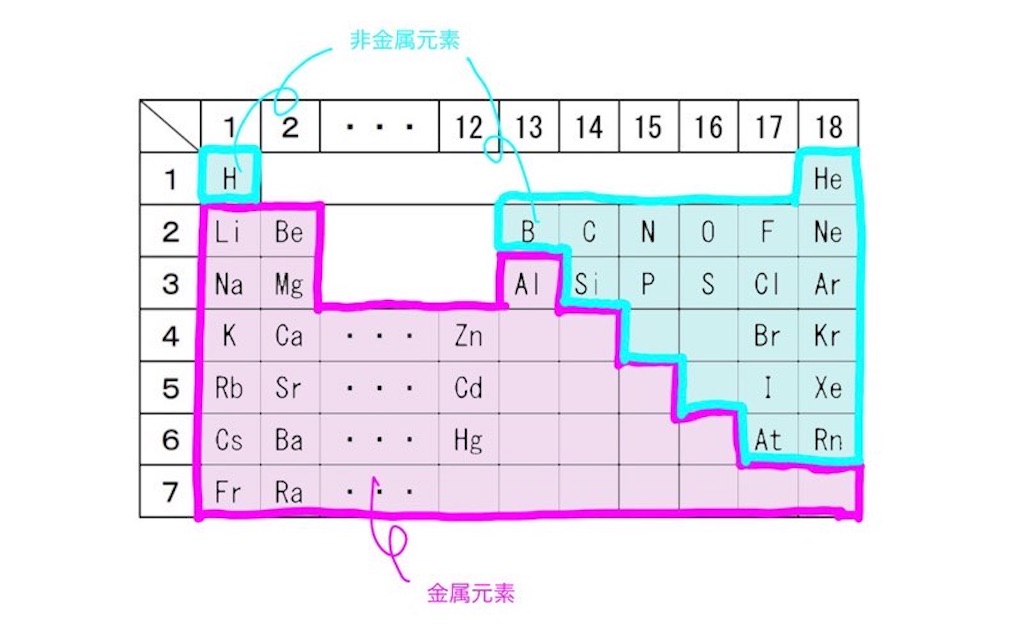
よって、結合の種類は、
の3種類に分類できます。
ここからはこの3つの結合と、4種類の結晶についてさらに詳しく見ていきたいと思います。
⭐︎ 結合と結晶の関係性

上の画像をもとに結合と結晶について見ていきたいと思います。
・ 金属結晶
金属元素どうしは、自由電子による金属結合によって繋がっています。
金属元素は基本的に価電子が1個から2個ですので、電子を放出して陽イオンとして存在しています。
放出された電子が自由電子となって、金属元素の陽イオンどうしを結びつけているわけです。
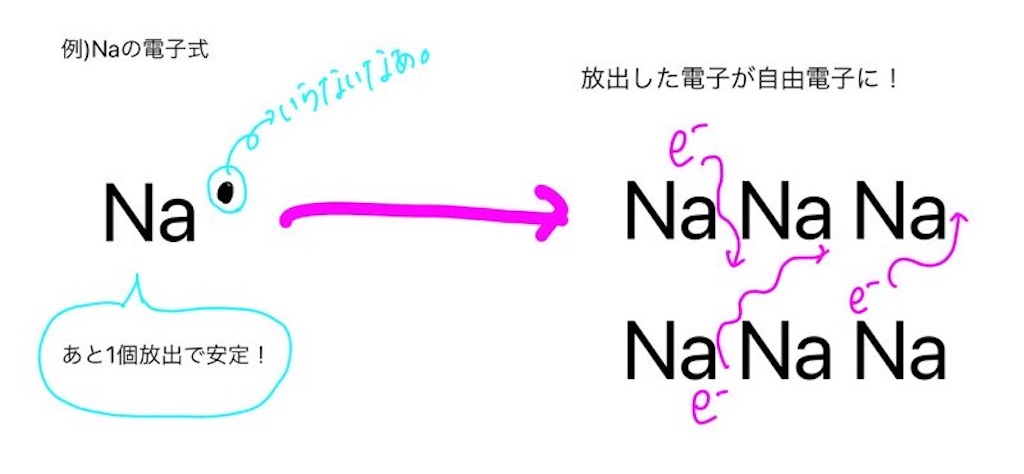
自由電子によって大量に金属元素の陽イオンが集合した結晶が金属結晶です。
金属結晶は
①展性・延性を持つ、②電気・熱伝導性がある、③金属光沢を持つ
という性質があります。
・ イオン結晶
金属元素の陽イオンと非金属元素の陰イオンの静電気力による結合が、イオン結合です。
非金属元素は、基本的には周期表の左側に位置しており、価電子が6〜7個をですので陰イオンになりやすいという特徴があります。
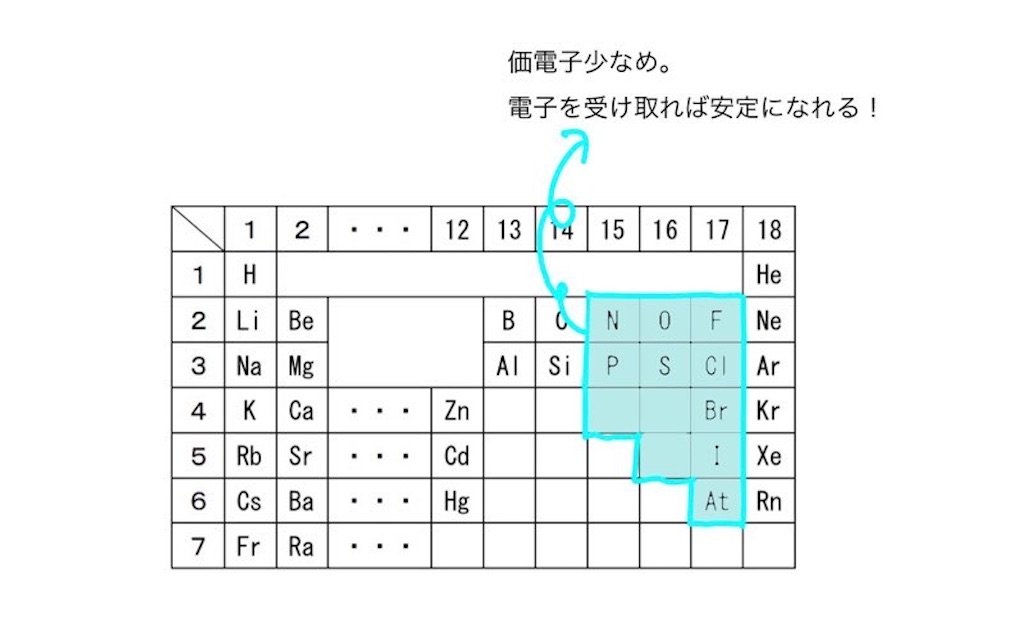
金属元素の陽イオンと非金属元素の陰イオンが静電気力によって大量に集合した結晶がイオン結晶です。
イオン結晶は
①硬いが割れやすい、②溶液は電気を通す、③融点が高い
という特徴があります。
・ 共有結合と分子結晶
非金属元素どうしが不対電子を出し合うと、共有結合を作ります。
ここで確認したいのは、共有結晶と分子結晶の違いです。
先に両者の違いについて結論を出しておくと、
共有結合性の結晶(共有結晶)は共有結合のみで非金属元素が集合してできた結晶
分子結晶は、共有結合によって非金属元素が分子を作り、分子がファンデルワールス力によって集合してできた結晶
となっています。
例)ヨウ素(分子結晶)
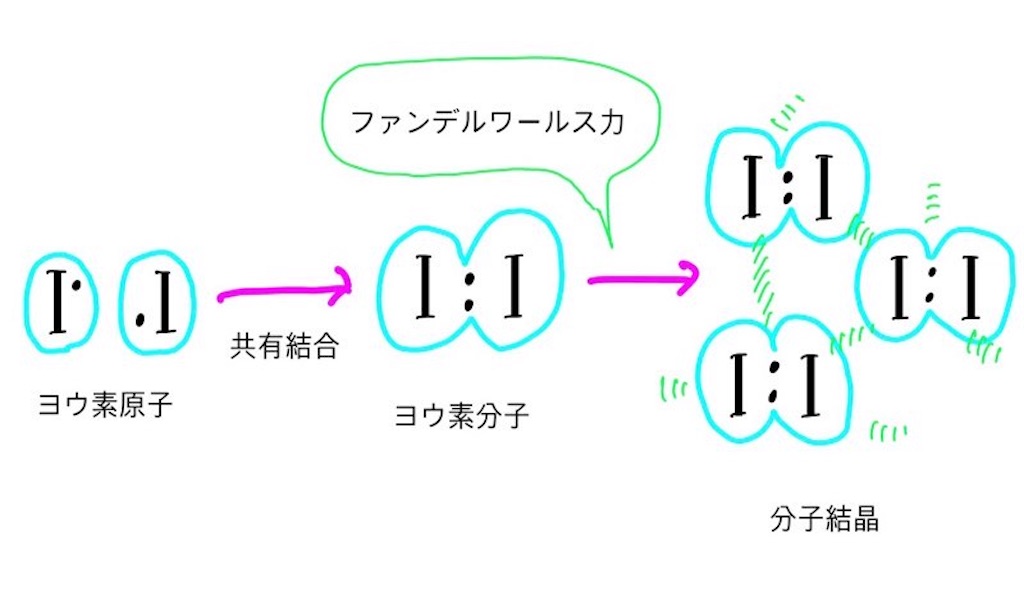
(ヨウ素のような分子結晶と違い、共有結晶はファンデルワールス力がありません。共有結合のみです。)
共有結合性の結晶は共有結合のみでできており、共有結合は非常に強力な結合ですので、
①融点が高い、②非常に硬い
という特徴を持ちます。
共有結合性の結晶を作る物質の代表例としては、ダイヤモンド、ケイ素、二酸化ケイ素があります。
この物質しか共有結合性の結晶はほぼないので、しっかりと覚えておきましょう。
分子結晶は、共有結合でまず分子を作り、その分子がファンデルワールス力という弱い引力によって集合した結晶です。
弱い引力で集合していますので、
①融点が低い、②やわらかい
という特徴を持っています。
⭐︎ 結合の強さの大小関係
結合の強さの大小関係は下のようになっています。
結合の強さと、融点・沸点の大小関係は比例します。
融点というのは、粒子がバラバラになる温度です。
結合力が強ければ強いほどバラバラになりづらいので、融点(沸点)は高くなります。
結合の大小関係を覚えておくと、融点や沸点、柔らかさなどの性質が丸暗記しなくてもわかるようになりますので、頭に入れておいたら便利です。
⭐︎ まとめ

化学の偏差値10アップを目指して、頑張りましょう。
またぜひ、当ブログにお越しください。