【高校化学】ダニエル電池の原理を徹底解説!ボルタ電池との違いや素焼き板の意味は?

世界で1番最初に実用化された電池であるダニエル電池。
ボルタ電池との違いや、素焼き板の意味など、混乱する受験生や化学学習者の方は多いはず。
今回はダニエル電池の原理と、素焼き板(半透膜)で電解液を分ける理由、ボルタ電池との違いを徹底解説したいと思います。
このブログを読めば、「素焼き板を取り除いたらどうなるのか。」「ダニエル電池を長持ちさせるためには?」など、受験で頻出する問題を考えて解けるようになっているはずです。
☆ ダニエル電池とは
ボルタ電池は世界で1番最初に作られた電池で、すぐに分極してしまうポンコツ電池でした。
ボルタ電池の記事はこちら↓
【高校化学】ボルタ電池の分極は間違い?実際に起こっている反応をご紹介 - 化学の偏差値が10アップするブログ
ボルタ電池に改良を重ね、世界で初めて実用化されるようになった電池がダニエル電池です。
ボルタ電池とダニエル電池の違いは、たった1つ
素焼き板(半透膜と表現することもあり)で電解液を分けているかいないか
です。
ダニエル電池は素焼き板で電解液を分けることによって、電池の起電力が長持ちします。
その理由は後々説明します。
電池で抑えておかなくはいけない電極の種類、電解液の種類は以下のようになっていますので、しっかりと確認しておいてください。
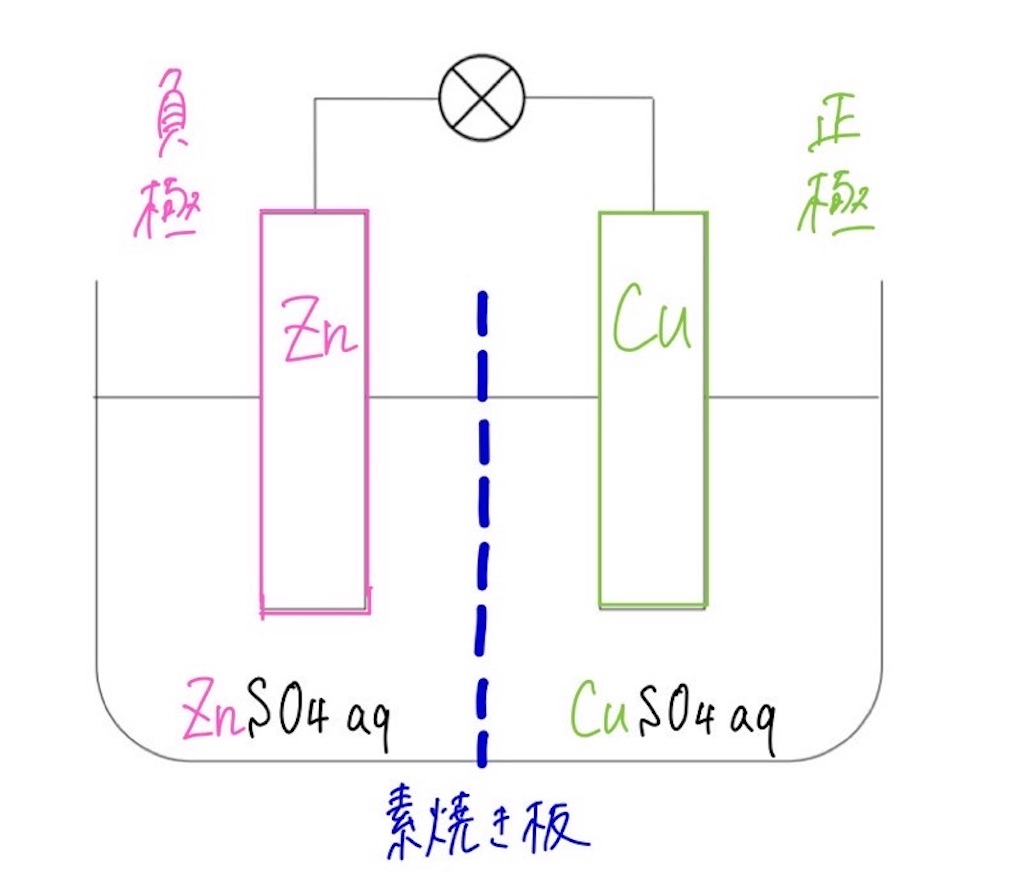
負極:亜鉛、正極:銅
見ての通り、ダニエル電池の電極はボルタ電池と全く同じです。
電解液と素焼き板の有無でなぜこんなにも違いが出てしまうのか、お伝えしていこうと思います。
☆ 素焼き板とは、素焼き板の性質
ダニエル電池の原理の前に、素焼き板とは何なのかを確認します。
素焼き板の性質は、電気分解や浸透圧の原理など、入試問題を解く上でとても大事ですので、絶対に押さえておいてください。
素焼き板(半透膜)とは
特定の粒子だけを通過させることのできる板(膜)となっています。
ここでのポイントは、どの粒子がどの方向に移動するのか、ということです。
一般的に、特別な要因がない限りは、粒子は素焼き板の反対側へと通過することができません。
下の図は、溶液に浸した素焼き板を拡大した図となっています。

粒子目線から見ると、素焼き板というのはとても分厚いのです。
粒子の熱運動だけでは、素焼き板の反対側の距離を移動することはできません。
(※溶液における熱運動では、です。)
ただし、素焼き板の反対側から、粒子を引っ張ってくれる力(=静電気的な引力)があれば、話は別です。

上の図は、素焼き板をはさんで右側の方がプラスの電荷が多くなっています。
つまり、左側のマイナスの電荷を持つ粒子は、右側のプラスに引っ張られて、左側から右側へと移動できるようになります。

素焼き板の役割は、溶液の電荷の総和がプラスマイナスゼロになるように、粒子を通過させることです。
電荷に偏りがある溶液が、電荷の偏りを打ち消すために反対符号の粒子を引きつけることによって、
粒子の選別をしながら、粒子が素焼き板を通過することができます。
このことを念頭に入れて、ダニエル電池の原理を見ていきたいと思います。
☆ ダニエル電池の原理
・ダニエル電池の基本的な反応
途中までは、ボルタ電池と同じです。
よって、負極が亜鉛で、正極が銅です。
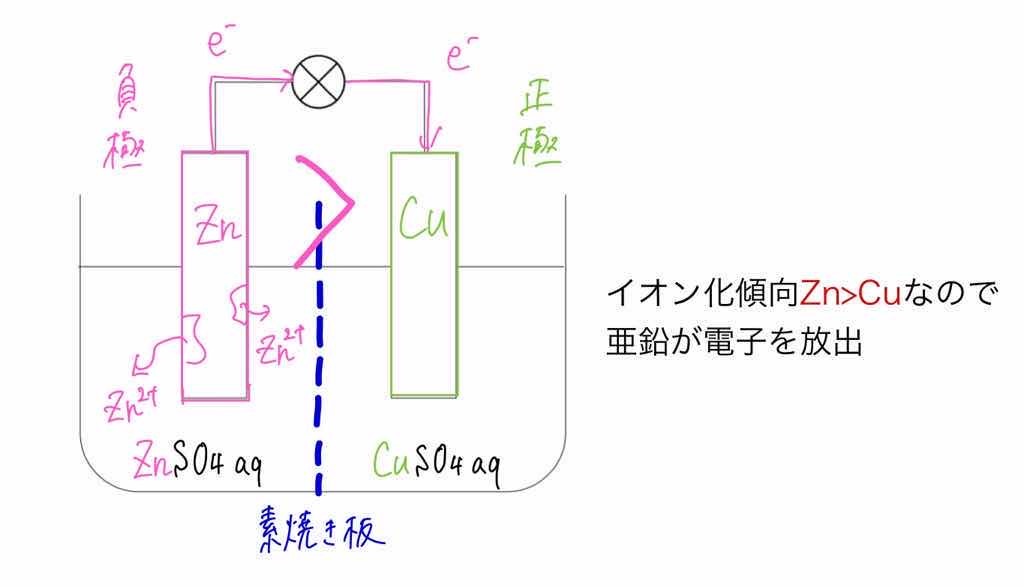
電池は、酸化還元反応によるエネルギーを外部に取り出したものです。
電子を放出する物質(この場合は亜鉛)がいたら、誰かが電子を受け取らなくてはいけません。
ただ、ボルタ電池で学習したように
→【高校化学】ボルタ電池の分極は間違い?実際に起こっている反応をご紹介 - 化学の偏差値が10アップするブログ
金属は電子を受け取る能力はないのでした。
金属は電子を受け取るのではなく、電子を放出して陽イオンになりたい物質です。
銅電極自身は電子を受け取れないので、電解液の誰かが電子を受け取らなくはいけません。
溶液には硫酸銅由来の銅イオンがあります。
よって、銅イオンが電子を受け取って、銅が析出するような反応が起きます。

気づいたでしょうか。
ボルタ電池と違って、水素分子が発生していません。
水素分子が電極を取り囲むこともないので、分極が起きません。
ダニエル電子は水素が発生しないので、分極が起きない
ボルタ電池よりもダニエル電池が長持ちする理由は、これになっています。
・素焼き板を設置する意味
素焼き板を設置する理由は2つあります
① 各極の電解液の混合を防ぐため
② 各極の電解液の電荷の総和をプラスマイナスゼロにするため
です。
ここで、先程の素焼き板の原理から、素焼き板をまたいで移動しているイオンは何なのかを確認してみたいと思います。
負極側の電解液では、亜鉛イオンが放出されているので、プラスの電荷が多くなっています。
正極側の電解液では、銅イオンが銅の単体へ変化しているので、プラスの電荷が消費されています。
すなわち、正極側の電解液はマイナスの電荷が多くなっていますね。

素焼き板をまたぐイオンの移動は、電荷の偏りによる静電気力に引き寄せられて、粒子が多い方から少ない方への移動が起こります。
つまりダニエル電池では
負極側の亜鉛イオン(陽イオン)が、正極側の硫酸イオン(陰イオン)に引き寄せられることによって、素焼き板をまたいでの移動が起こっています。

素焼き板によって、適切なイオンの移動が起こり、各電解液の電荷の総和がゼロに保たれているのです。
もし素焼き板がなく、適切ではないイオンの移動、すなわち、
正極側の銅イオンが負極側へ移動するような反応が起こったらどうなるでしょうか。
素焼き板がなかったら、負極側には放出された亜鉛イオンとともに、銅イオンも存在することになります。
イオン化傾向は亜鉛>銅なので、銅イオンが銅の単体に戻るような反応が起きてしまいますね。
すると、このように

負極の電極だけで酸化還元反応が成立してしまい、外部へと電子(エネルギー)が出て行かなくなります。
電池として機能するには、素焼き板によって適切なイオンの移動を促すのが大切だということがわかります。
☆ ダニエル電池を長持ちさせるには
反対に、ダニエル電池が寿命を迎える時というのは
・ 亜鉛がイオンとなって溶け出せなくなる
・ 銅イオンが全て消費され、電子を受け取る物質がいなくなる
のどちらかです。
亜鉛がイオンとなって溶け出せなくなるのは、電解液に存在する亜鉛イオンが多すぎる時です。
一定量の亜鉛イオンが電解液へと溶けると、飽和状態(最大量の溶質が溶けた溶液を「飽和」水溶液といいますね。)になり、これ以上亜鉛がイオンとなって溶け出せなくなってしまいます。
銅イオンが全て消費されるというのはわかりやすいですね。
銅イオンが電子を受け取り銅の単体になることによって、電子を受け取る電解液中の銅イオンが少なくなってしまうわけです。

これらのことをなるべく起きないようにする
つまり、電池の寿命を長くするためには
そうすると、溶け出せる亜鉛イオンの量も増えますし
電子を受け取ることのできる銅イオンの量も増加します。
このように電解液の濃度により、電子のやり取りを促進した電池を濃淡電池といいます。
☆ まとめ
ダニエル電池は
素焼き板で電解液を仕切り
負極:亜鉛、正極:銅
で作成された電池である。
素焼き板を設置する理由は
・電解液の不適切なイオンの混合を防ぐため
・電解液の電荷の総和をゼロにするため
である。
化学の偏差値10アップを目指して、頑張りましょう。
またぜひ、当ブログにお越しください。